Introduction
- Bicarbonate HCO3-
- Omniprésent à l’état physiologique
- Couple Bicarbonate / Acide Carbonique : HCO3- + H+ ↔ H2CO3 ↔ CO2 + H2O
- L’Anhydrase Carbonique est l’enzyme qui catalyse ces réactions
- [H+] = déterminant primordial des fonctions physiologiques
En pratique, on utilise plutôt le potentiel Hydrogène ou pH = – log[H+]
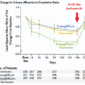
- Régulation fine du pH plasmatique : acidémie < pH normal 7,40 +/- 0,02 < alcalémie
- Attention : possibilité de pH normal avec processus pathologique en cours : acidose sans acidémie.
Par ex acidose respiratoire (acides volatiles issus du C02), ou acidose métabolique (baisse des bicarbonates plasmatiques)
- Régulation du pH par le couple acide carbonique/ bicarbonate (H2CO3/HCO3-)
- principal tampon extracellulaire en physiologie humaine1
- capacité à (re)générer ce tampon = enjeu majeur de l’organisme
1 – Alka K, Casey JR. Bicarbonate transport in health and disease. IUBMB Life. 2014;66(9):596-615. doi:10.1002/iub.1315