BJN spéciale SFT juniors #2: quoi neuf côté CMV?
En 2024, la SFT juniors a pu proposer des bourses pour que des jeunes médecins et scientifiques impliqués en transplantation d’organe puissent aller présenter leurs travaux à l’ESOT 2024 à Athènes.
En collaboration avec la SFT juniors, les récipiendaires de ces bourses vous proposent cette semaine une série de résumés de communications auxquelles ils ont pu assister à l’ESOT. N’hésitez pas à vous informer sur la SFT juniors!
Aujourd’hui, trois communications orales sur le CMV vous sont proposées.
1ère communication:
L’infection à CMV augmente le risque de maladie thromboembolique veineuse chez le transplanté rénal.
Une communication de Christophe MASSET, de Nantes, rapportée par Manal Mazloum, de Montpellier.
Contexte
Des complications thromboemboliques veineuses ont été retrouvées chez des patients atteints d’une infection CMV en contexte de transplantation rénale. Par ailleurs, d’anciennes données in vitro semblent montrer que l’adhésion plaquettaire est augmentée à la surface de cellules endothéliales infectées par le CMV.
L’objectif de cette étude était d’évaluer l’association entre infection à CMV et survenue des évènements thromboemboliques veineux en transplantation rénale.
Méthodes
Au total, 13943 patients issus de la cohorte DIVAT étaient inclus dans l’étude entre 2000 et 2021. L’incidence cumulée d’infections à CMV et d’évènements thromboemboliques veineux était ensuite déterminée dans les deux premières années suivant la transplantation rénale.
Les auteurs ont utilisé un modèle de Cox afin de déterminer les facteurs de risque d’évènement thromboembolique veineux.
Résultats
La présence d’une infection asymptomatique et d’une maladie à CMV augmentait significativement le risque ultérieur d’évènement thromboembolique veineux de 61 et 100 %, respectivement. De façon intéressante, 40% des patients avaient une infection à CMV concomitante d’un évènement thromboembolique veineux.
Perspectives / Implications
Le risque de maladie thromboembolique veineuse est augmenté en présence d’une infection à CMV chez le transplanté rénal. Ce résultat doit motiver les cliniciens à prendre en compte ce risque ainsi qu’à dépister l’infection CMV devant toute complication thromboembolique veineuse sans cause évidente du transplanté rénal.
2ème communication:
Prévalence de la résistance du CMV aux antiviraux chez les patients transplantés.
Il s’agit d’une communication de Steve Kleiboeker, Lee’s Summit, USA, rapportée par Salhi Sofiane, de Toulouse.
Contexte:
La résistance du CMV est bien documenté pour les différents anti-viraux et la recherche de résistance est réalisée après persistance d’une réplication virale ou d’une maladie à CMV après 6 semaines de traitement. Ici est rapporté la résistance au CMV en fonction du type de traitement administré.
Méthodes:
2750 échantillons ont été analysés au laboratoire EUROFINS VIRACOR pour le ganciclovir, le foscarnet, le maribavir, le cidofovir et le letermovir. Les gènes UL54, UL56 et UL97 étaient amplifiées par PCR puis les résistances recherchées par séquencage par méthode Sanger.
Résultats :
95 génotypes mutés ont été retrouvés, le plus fréquemment concernant UL97. Dans 27,6% des cas, était retrouvée une mutation UL97 liée au ganciclovir et 9,9% liée au maribavir. Les mutations de résistance UL54 étaient positives dans 6, 1,8 et 6,1% respectivement pour le cidofovir, le foscarnet ou le ganciclovir Le letermovir, quant à lui, était associé à une mutation UL56 dans 7% des cas. L’incidence cumulée totale de résistance liée au ganciclovir était de 29,7%.
7,8% des patients présentaient une résistance à deux traitements (en général cidofovir et ganciclovir ou maribavir et ganciclovir). 1% des patients avaient une résistance à trois traitements (ganciclovir, cidofovir, foscarnet ou letermovir) et seulement 0,18% des patients avaient une résistance à 4 traitements (ganciclovir, cidofovir, foscarnet, maribavir majoritairement). Les mutations les plus fréquentes de UL97 concernant le ganciclovir regroupaient L595S, A594V et C603W. Certaines mutations conféraient une résistance contre le ganciclovir et le maribavir (F382Y et C480F). Les mutations UL56 pour le letermovir concernaient principalement le domaine C325 qui entraînait une résistance absolue.
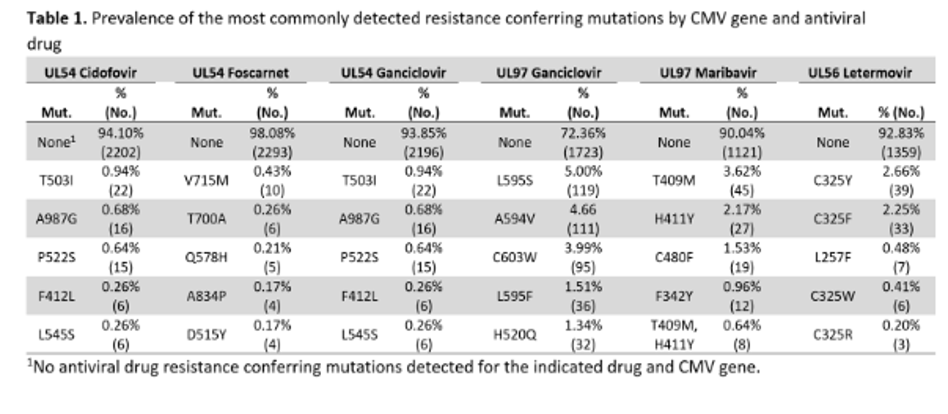
Perspectives:
Les mutations entraînant une résistance au CMV étaient retrouvées dans 30% des échantillons envoyés pour recherche de génotypage. Bien que de nombreuses mutations existent, un nombre limité de mutations représente l’essentiel des mutations retrouvées chez les patients. Un tiers des patients résistants portait une résistance à un autre traitement anti-viral. Des tests de recherche de résistance complet, rapides et sensibles sont nécessaires au vue du risque de résistance envers un autre traitement anti-viral.
3ème communication:
Burden of refractory/resistant cytomegalovirus or cytomegalovirus drug intolerance in solid organ transplant recipients: european subgroup analysis,
Une communication de E. A. Blumberg, Philadelphia, USA, rapportée par Adelaïde Sanson, de Paris
Contexte:
L’infection à CMV est une complication fréquente après une transplantation d’organe solide. L’objectif de l’étude est d’analyser les infections à CMV réfractaires au traitement, et l’intolérance des patients aux traitements conventionnels.
Méthode :
Il s’agit d’une étude rétrospective multicentrique conduite par une équipe américaine, mais incluant les données de 8 centres européens. Les patients étaient inclus s’ils avaient un antécédent de transplantation d’organe solide après janvier 2014, et un diagnostic d’infection à CMV considérée comme résistante (avec identification d’une mutation génétique de UL54, UL97 ou UL27), réfractaire (échec de contrôle de la virémie malgré absence de mutation identifiée et bonne observance du traitement à bonne posologie) ou avec une intolérance à un des traitements conventionnels (RRI).
Résultats :
112 patients ont été inclus dans l’étude. La durée moyenne de follow up était de 3 ans. Pour 97% des patients, la première infection à CMV était d’emblée considérée comme RRI.
La durée médiane entre la transplantation et le premier épisode d’infection à CMV était de 94 jours.
Parmi les intolérances au traitement, une des plus fréquentes était la myélotoxicité du valganciclovir (74% des patients sous valganciclovir).
53% ont eu besoin d’au moins deux différents traitements anti CMV. 22% des patients n’ont pas eu de négativation de leur virémie pendant la RRI. 19% ont eu une récurrence d’infection à CMV.
La mortalité toute cause était de 22% dans la durée de follow up.
Conclusion :
Cette étude montre que les infections à CMV sont difficiles à traiter, avec des traitements mal tolérés, et insiste sur la nécessité de nouvelles thérapies permettant de contrôler la virémie tout en évitant les effets indésirables trop fréquents.