BJN#177 – Le Rituximab, ça vous défibrille ?
Cet article du BJN est rédigé en rapport avec les références bibliographiques suivantes :
Erickson SB, Zand L, Nasr SH, Alexander MP, Leung N, Drosou ME, Fervenza FC. Treatment of fibrillary glomerulonephritis with rituximab: a 12-month pilot study. Nephrol Dial Transplant. 2020 Jul 2:gfaa065. doi: 10.1093/ndt/gfaa065. Epub ahead of print. PMID: 32617582.
Lien vers l’article : Treatment of fibrillary glomerulonephritis with rituximab: a 12-month pilot study
Merci à Cécile Teuma, Néphrologue à Lyon, membre du Comité Scientifique du CJN, pour cette synthèse bibliographique. Vous aussi, n’hésitez pas à nous envoyer vos lectures !
Introduction
La glomérulonéphrite fibrillaire (GNF) est une cause rare de syndrome glomérulaire avec IRC se caractérisant à la biopsie rénale par la présence de dépôts mésangiaux non colorés par le Rouge Congo et organisés en disposition fibrillaire en ME, avec présence d’IgG et de complément en IF. Bien que plusieurs thérapies immunosuppressives (IS) aient déjà été tentées, elle est associée à un mauvais pronostic rénal en l’absence de traitement efficace à ce jour (corticostéroïdes, cyclophosphamide, anticalcineurines, mycophenolate mofetil, azathioprine, inhibiteur du protéasome). Le plus souvent idiopathique, une cause secondaire n’est retrouvée que dans 40% des cas (gammapathie monoclonale, néoplasie, pathologies auto immunes ou virales). Le but de cette étude pilote était d’étudier l’impact du Rituximab dans l’évolution du DFG et de la protéinurie chez les patients atteints de GNF idiopathiques.
Patients/matériels et méthodes
Étude prospective menée de 2014 à 2016 à la Mayo Clinic, au sein de patients âgés de 18 à 79 ans, non diabétiques et normotendu, avec diagnostic d’une GNF à bilan étiologique négatif dans les 2 années écoulées sans traitement IS depuis au moins 6 mois. Le DFG devait être > 25 ml/min et la protéinurie d’au moins 1g/24h sous IEC ou ARAII. Tous les patients recevaient 1g de Rituximab IV J1-J15 à T0 puis 6 mois plus tard. Les co-médications comprenaient du paracétamol, un anti histaminique et 100 mg de methylprednisolone en prémédication puis Bactrim en prophylaxie de la pneumocystose. Les patients étaient évalués cliniquement et biologiquement avec dosage de la créatininémie, du biomarqueur DNAJB9, des sous-populations lymphocytaires et recueil de la protéinurie des 24h à 1 mois, puis tous les 3 mois pendant les 12 mois de l’étude. Le critère de jugement principal était la préservation de la fonction rénale à 12 mois avec une clairance de la créatininémie stable ou en hausse. Le critère secondaire était la rémission complète (RC) de la protéinurie < 300 mg/24h, ou partielle (RP) <3 g/24 h et 50% réduction de la protéinurie basale.
Résultats
11 patients de 59 ans en moyenne ont été inclus, en moyenne 2 ,9 mois après le diagnostic de GNF à bilan étiologique négatif et ont été tous suivis pendant 12 mois. Tous les patients sauf 1 étaient sous bloqueur du SRA, et 9 des 11 patients étaient naïfs de tout traitement IS. Au terme de l’étude, il n’y avait pas de différence significative entre les créatininémies pré thérapeutiques et à 1 an (176 vs 140 micro/L, p= 0,15), tendance non significative à la baisse de la protéinurie (1,9 vs 4,42 g/24h p=0,06) avec une grande variabilité entre les patients (Figures 1 et 2). Plus de la moitié des patients avaient une baisse du DFG < 15% de la valeur de base. A 1 an, il n’y avait aucun patient en rémission complète, 3 patients étaient classés en RP avec 8 patients non répondeurs dont un qui présentaient une réduction de la protéinurie de 44% et une amélioration du DFG de 39 à 53 ml/min/1,73m2. La déplétion lymphocytaire était efficiente chez tous les patients à 1 mois, et persistait à 12 mois sauf pour 2 patients en RP. La tolérance du Rituximab était bonne avec comme principaux effets secondaires une asthénie, une congestion nasale et des crampes. Les taux de DNAJB9 étaient inversement proportionnels au eDFG, et stables pendant les 12 mois de suivi, sans différence y compris chez les 3 patients en RP.
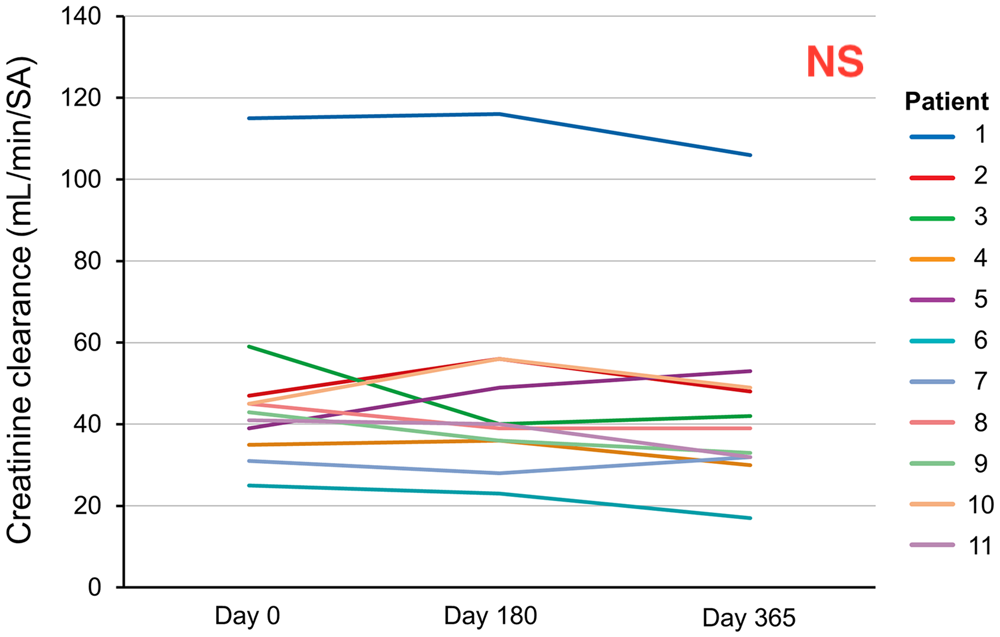
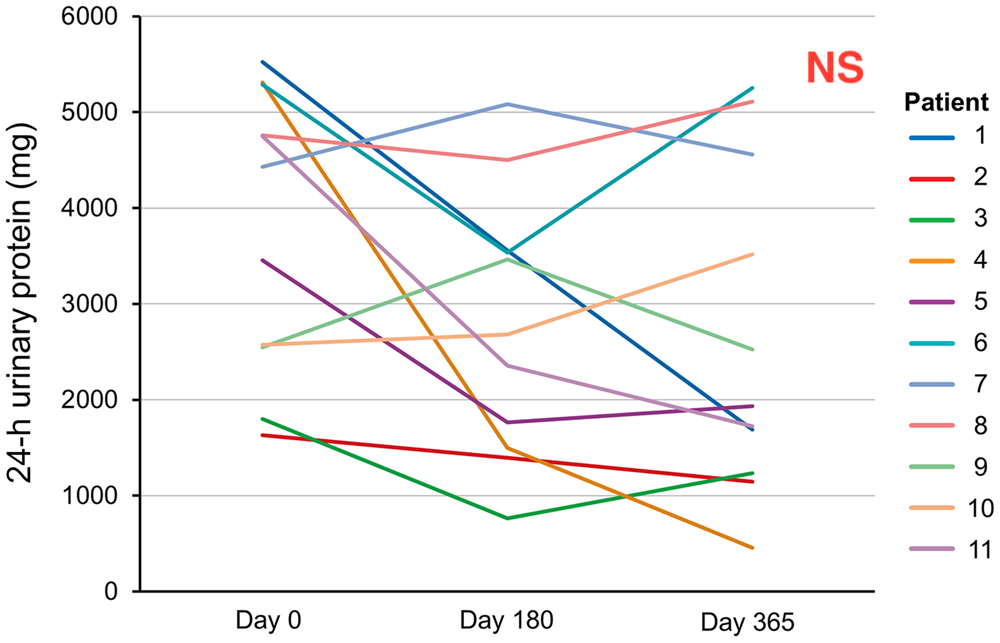
Conclusion
Stabilisation de la fonction rénale avec absence de différence significative sur la créatininémie, la clairance de la créatinine ou le DFG à 12 mois après 4 doses de Rituximab à 6 mois d’intervalle, baisse non significative de la protéinurie de 56% en dépit d’une déplétion lymphocytaire efficace. Pas d’effet direct du Rituximab sur le taux de DNAJB9.
Les plus du papier
- Étude pilote avec peu de patients mais une cohorte cohérente avec les autres études sur cette pathologie rare dans la littérature
- Élargissement des hypothèses sur rôle de DNAJB9 dans la physiopathologie
Les critiques
- Définition des RP et RC utilisées dans cette étude non validées officiellement dans cette pathologie
- Pas de groupe contrôle
- Durée de suivi insuffisant pour juger de l’efficacité à moyen terme sur la protéinurie ou le pronostic rénal (3 des 8 patients non répondeurs à 12 mois ont baissé leur protéinurie dans les suites, et un patient a démarré la dialyse 3 mois après la fin de l’étude), ou conclure sur l’effet potentiellement pathogénique du DNAJB9.

