BJN#190 – Réponse anti-virale en transplantation : monitorer les CD4, pour un traitement à la carte
Cette BJN est rédigée en rapport avec la référence bibliographique suivante :
Ahlenstiel-Grunow T, Liu X, Schild R, Oh J, Taylan C, Weber LT, Staude H, Verboom M, Schröder C, Sabau R, Großhennig A, Pape L. Steering Transplant Immunosuppression by Measuring Virus-Specific T Cell Levels: The Randomized, Controlled IVIST Trial. J Am Soc Nephrol. 2021 Feb;32(2):502-516. doi: 10.1681/ASN.2020050645. Epub 2020 Dec 15. PMID: 33323473.
Lien vers l’article : Steering Transplant Immunosuppression by Measuring Virus-Specific T Cell Levels: The Randomized, Controlled IVIST Trial
Merci à Tristan de Nattes, Néphrologue à Rouen, membre du Comité Scientifique du CJN, pour cette synthèse bibliographique. Vous aussi, n’hésitez pas à nous envoyer vos lectures !
Introduction
A ce jour, le monitorage des immunosuppresseurs en transplantation rénale repose sur les dosages de résiduelles devant être dans des cibles non individualisées. Cette stratégie expose au risque de sur-immunosuppression (complications virales, oncologiques, métaboliques…).
Dans cet essai randomisé, les auteurs ont évalué l’intérêt d’utiliser le nombre de lymphocytes T CD4+ virus-spécifiques (Tvis) anti-CMV, anti-EBV et anti-Adénovirus afin de moduler les posologies d’immunosuppresseurs, en association aux mesures usuelles.
Patients/matériels et méthodes
- Patients:
Essai multicentrique allemand, 2010-2017, intention de traiter, population pédiatrique (11 ans en moyenne) avec ses spécificités :
- Population peu immunisée (pas de DSA, peu de missmatch en -A, -B et -DR)
- Sérologie IgG-EBV positive chez 54.0% des patients, sérologie IgG-CMV positive chez 35.9% des patients
- Exclusion des patients avec un PRA > 50%
- Protocole d’immunosuppression: induction basiliximab, entretien everolimus + ciclosporine + corticoïdes
- Intervention: randomisation à 4 semaines post transplantation.
- Groupe intervention (31 patients) : Mesure du nombre de T CD4+ anti-CMV, -EBV et -ADV à 4, 6, 8, 10 et 12 semaines post-transplantation, puis tous les mois jusqu’à M12, puis tous les 2 mois jusqu’à M24. La détermination des T CD4+ spécifiques était faite en mesurant le taux de CD4+ spécifiques activés après stimulation antigénique in vitro.
- Si nombre de Tvis inférieur au seuil : diminution des posologies d’immunosuppresseurs de 10 à 15%
- Si nombre de Tvis supérieur au seuil : majoration des posologies d’immunosuppresseurs.
- Groupe contrôle (31 patients): suivi habituel.
Résultats
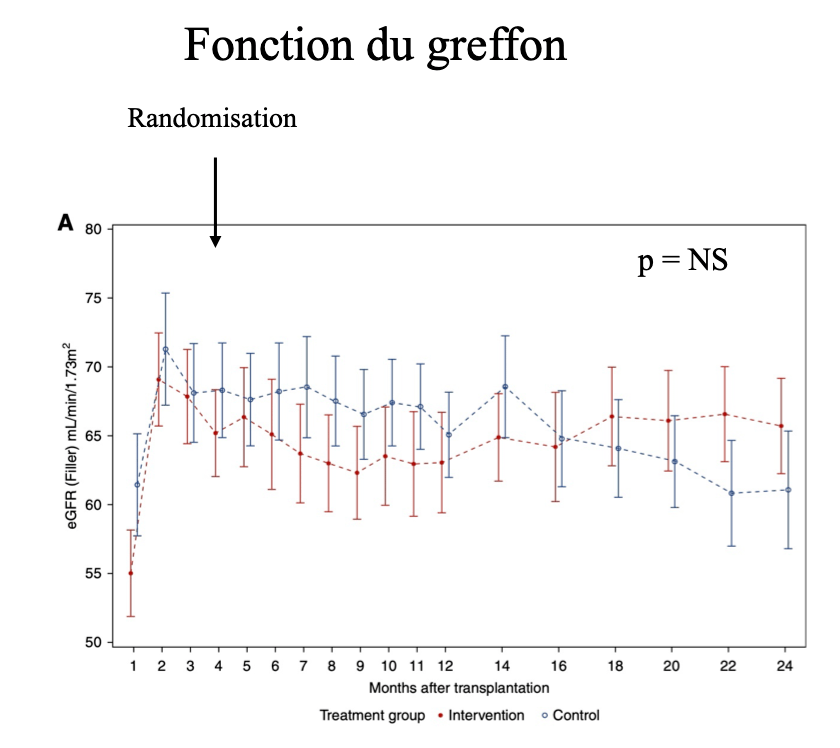
- Critère jugement principal: absence de différence de fonction du greffon à 2 ans (figure 1)
- Groupe intervention : eGFR passant de 55.0 ± 17.5 lors de la randomisation à 60.7 ± 22.8 mL/min/1.73m2 à deux ans (pas de différence significative)
- Groupe contrôle : eGFR passant de 61.5 ± 21.3 à 59.6 ± 22.3 mL/min/1.73m2, pas de différence.
- Absence de différence entre les deux groupes à ces différents endpoints.
 Critères de jugement secondaires:
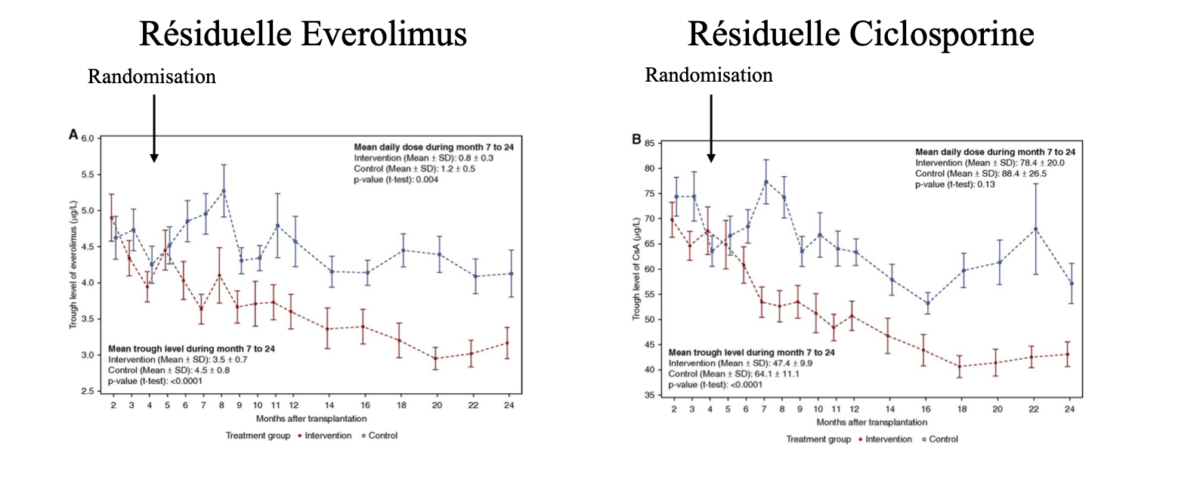
Critères de jugement secondaires:
- Diminution des résiduelles d’everolimus et de ciclosporine dans le groupe intervention (3.5 ± 0.7 versus 4.5 ± 0.8 µg/L, p < 0.001 et 47.4 ± 9.9 versus 64.1 ± 11.1 µg/L, p < 0.001), (figure 2)
- A deux ans, plus de sevrage en corticoïdes dans le groupe intervention (80% versus 53%, p = 0.04)
- Pas de différence d’incidence de DSA de novo à 1 an (25.8% versus 27.3%, p = 0.89)
- Pas de différence de survenue de rejet aigu entre les groupes (29% groupe intervention versus 49%, p = 0.1)
- Nombre de CMV-virémie et de néphrite à BK virus similaire dans les deux groupes
- Tendance à plus de réplication EBV dans le groupe contrôle (42% versus 23%, p = 0.09)
- Pas de différence de nombre d’évènements indésirables entre les groupes.
 Conclusion
Conclusion
L’ajout de l’évaluation des lymphocytes T CD4+ virus-spécifiques dans le monitorage et l’adaptation des posologies d’immunosuppresseurs en transplantation rénale pédiatrique n’a pas d’effet sur la fonction du greffon à 2 ans. Cette évaluation permet de diminuer les posologies d’everolimus, ciclosporine et corticoïdes, sans sur-risque de rejet, de DSA de novo ou de virémie à CMV.
Les plus du papier
- Essai randomisé
- Cet article souligne l’importance d’identifier les patients sur-immunosupprimés et de la nécessité de mieux personnaliser les posologies d’immunosuppresseurs chez les patients transplantés rénaux.
- La baisse des immunosuppresseurs guidée par la réponse anti-virale parait sure en termes de fonction greffon à 2 ans et de survenue de rejet aigu.
Les critiques
- Population pédiatrique avec ses spécificités, peu d’immunisation, protocole d’immunosuppression everolimus + ciclosporine.
- Recrutement de 2010 à 2017 avec risque de modifications des pratiques sur cette période.
- Survenue des complications des effets secondaires des IS peu détaillée ; les auteurs prévoient un article à 5 ans pour les évaluer.
- Peu de détails sur les caractéristiques des DSA de novo. Pas de détails sur les biopsies réalisées, en particulier sur d’éventuelles lésions humorales.