Plusieurs mécanismes contribuent à amplifier et à pérenniser la réponse inflammatoire.
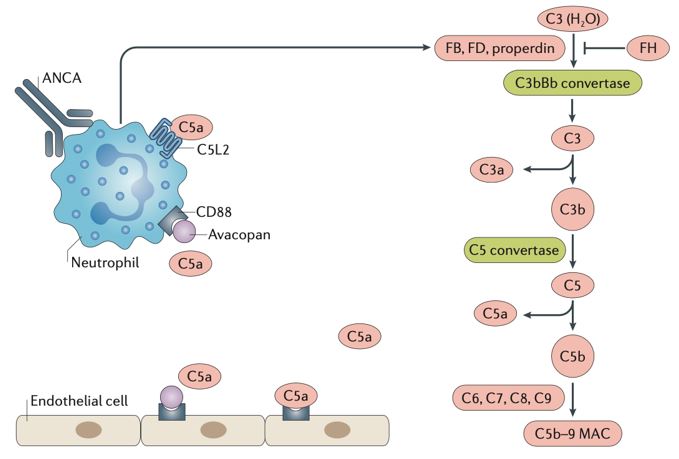
A. Rôle central de la voie alterne du complément (Figure 2)
Les neutrophiles activés par les ANCA libèrent des facteurs (tels que la properdine), qui amplifient l’activation de la voie alterne du complément, générant de grandes quantités de C5a.
- Le C5a est une anaphylatoxine puissante, dotée d’une activité chimiotactique, qui recrute de nouveaux neutrophiles au site inflammatoire.
- En se liant à son récepteur (C5aR1/CD88) à la surface des neutrophiles, il agit comme un signal de priming majeur, renforçant la sensibilité des neutrophiles à l’activation par les ANCA.
Cette boucle auto-entretenue – activation des neutrophiles induisant activation du complément, lequel amplifie à son tour l’activation neutrophilique – joue un rôle fondamental dans la physiopathologie des VAA. Sa mise en évidence a conduit au développement de stratégies thérapeutiques ciblées, notamment l’inhibiteur du C5aR1 Avacopan, qui bloque la voie pro-inflammatoire (C5a–C5aR1) tout en préservant l’interaction C5a–C5L2, à fonction anti-inflammatoire.
B. Contribution de l’immunité adaptative
- Lymphocytes B: au-delà de la production d’ANCA, ils participent à la présentation d’antigènes aux lymphocytes T. Leur survie est renforcée par le facteur de survie BAFF (B-cell activating factor), sécrétés notamment par les neutrophiles activés.
- Lymphocytes T CD4+: les sous-populations Th1 et Th17 jouent un rôle majeur. Les Th1 produisent de l’IFN-γ, activant macrophages et cellules effectrices, tandis que les Th17 sécrètent de l’IL-17, favorisant le recrutement de neutrophiles et la chronicisation de l’inflammation. Ces mécanismes contribuent également à la formation de granulomes, caractéristiques de la GPA.







