BJN#271 – La génétique gériatrique c’est chic !
Merci à Marion Delafosse de PARIS, (ex) membre du conseil scientifique pour ce résumé.
N’hésitez pas, si vous le souhaitez, à nous envoyer vos lectures !
Cette BJN est rédigée en rapport avec cet article :
Characterization of Monogenic Kidney Disease in Older Patients With CKD , Elhussein A et al. Kid Int Reports
Introduction
La génétique est en plein essor et 10% à 15% des insuffisances rénales chroniques (IRC) sont attribuables à des causes monogéniques chez l’adulte. Néanmoins leur part dans des populations « âgées » (> 60ans) est mal caractérisée. L’objectif de cette étude est de décrire les IRC d’origine monogénique chez des patient(e)s âgé(e)s et de voir si le diagnostic amenait à une modification de la prise en charge.
Matériels et méthodes
L’étude a été réalisée à partir d’une cohorte observationnelle irlandaise de patient(e)s ayant bénéficié entre 2014 et 2023 d’une analyse génétique pour suspicion de néphropathie monogénique ou devant une insuffisance rénale d’origine indéterminée. Les patient(e)s âgé(e)s de 60ans et plus au moment du prélèvement étaient inclus dans l’étude (cas index ou apparenté).
Résultats
Sur les 995 adultes de la cohorte, 265 patient(e)s de 202 familles ont été inclus(e)s, avec un âge médian de 71ans. L’âge médian au diagnostic de la maladie rénale était de 44ans. Une histoire familiale de néphropathie était retrouvée dans 83.7% des cas.
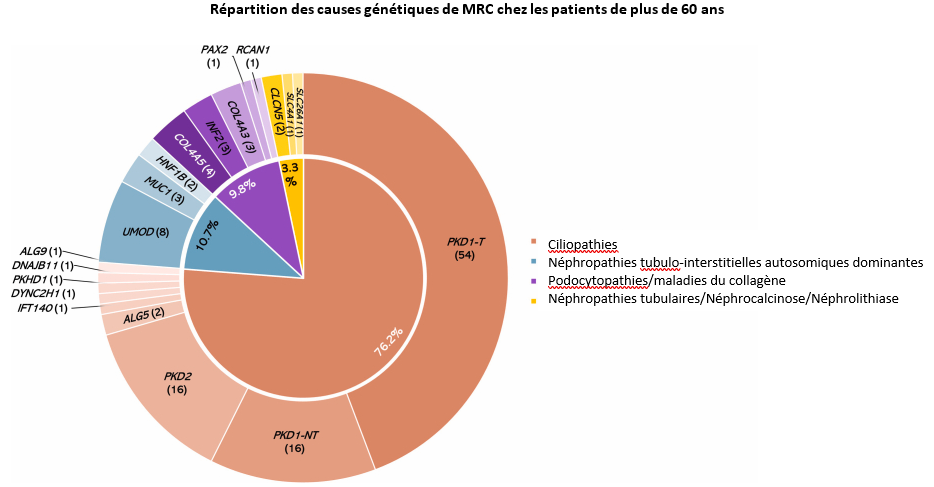
Un variant pathogène était retrouvé dans 60.4% des familles. Les gènes les plus fréquents étaient ceux de la polykystose rénale autosomique dominante (PKD1 : 57.4% PKD2 : 13.1% des cas), des gènes associés aux néphropathies tubulo-interstitielles chroniques (UMOD 6.5%) et aux basalopathies (COL4A5 : 3.3% et COL4A3 2.4% des cas).
Dans le sous groupe des patient(e)s avec un début de la maladie après 60ans (n=55), l’analyse génétique était positive dans 54.5% des cas. Les variants associés avec ces phénotypes tardifs appartenaient au spectre de la polykystose rénale autosomique dominante (ALG5, ALG9, DNAJB11, IFT 140) ainsi qu’aux gènes UMOD (variant p.Thr62Pro) et COL4A3.
Les facteurs prédictifs d’avoir un diagnostic positif dans cette population étaient d’avoir une histoire familiale de maladie rénale chronique (p<0.001) ou une suspicion de maladie kystique (p = 0.005) ou tubulo interstitielle (p = 0.012).
Le diagnostic génétique entrainait un dépistage des apparentés dans 73.7% des cas et modifiait le traitement proposé dans 24% des cas.
Conclusion
Même dans une population âgée (mais sélectionnée), l’analyse génétique peut être contributive dans un nombre non négligeable de cas, et contribue à modifier la prise en charge des patients. Il ne faut donc pas hésiter à explorer ces patients sur le plan génétique notamment en cas d’antécédents familiaux.
Les plus du papier
Etude qui s’intéresse aux plus de 60ans, ce qui semble un peu contre-intuitif pour rechercher une maladie monogénique…mais finalement à raison !
Recueil du diagnostic supposé à priori, qui permet ensuite de voir dans quels cas la génétique est la plus contributive.
Les critiques
Population très sélectionnée avec 60% de causes génétique retrouvée, alors que la prévalence est plutôt de 15% dans d’autres cohortes s’étant intéressées également aux sujets âgés. 70% des cas sont attribuables à une PKRAD dont le diagnostic peut souvent être fait sans génétique en cas d’histoire familiale, ce qui explique probablement en partie cette forte prévalence. Par ailleurs patients prélevés après 60 ans mais diagnostic de la maladie rénale souvent bien plus précoce (44ans) ce qui ne correspond pas tout à fait à une population gériatrique (sauf selon les critères CJN !)
Etude réalisée en Irlande, avec des patient(e)s exclusivement caucasiens, ce qui limite l’extrapolabilité des résultats










