BJN#101 – Eculizumab dans le SHU atypique : Stop ou encore ?
Safety and effectiveness of restrictive eculizumab treatment in atypical haemolytic uremic syndrome
Merci à Thibault Dolley-Hitze, Néphrologue à Saint-Malo et membre du Conseil Scientifique du CJN, pour cette synthèse bibliographique. Vous aussi, n’hésitez pas à nous envoyer vos lectures !
Introduction
L’utilisation de l’éculizumab a révolutionné le pronostic des patients développant un syndrome hémolytique et urémique atypique (SHUa). Les recommandations actuelles incitent à poursuivre à vie ce traitement alors que les conséquences au long cours ne sont pas connues et que le coût est prohibitif tandis qu’une récidive n’est pas certaine. Il est donc licite de s’interroger sur la poursuite de ce traitement.
Patients/matériels et méthodes
Il s’agit d’une étude rétrospective monocentrique néerlandaise qui décrit tous les patients qui ont présenté un SHUa et ont été traités par eculizumab. Le diagnostic de SHUa a été établi après avoir éliminé un SHU typique (shiga-toxine, déficit en ADAMST13, HTA maligne, grossesse, infection virale). Une recherche d’anticorps anti-facteur H et une analyse génétique pour rechercher une mutation des facteurs de régulation du complément ont été effectuées chez tous les patients suspectés de SHUa. Après obtention d’une rémission hématologique suite au traitement par éculizumab et après évaluation, le traitement a été espacé puis stoppé en l’absence de signe de rechute. En cas d’arrêt, les signes de rechute ont été recherchés toutes les 2 à 4 semaines pendant 4 mois puis tous les 2 mois. Les patients transplantés rénaux ont reçu un contrôle intensif de leur HTA et une minimisation des anticalcineurines. En cas de récidive clinique ou hématologique le traitement par éculizumab a été redémarré immédiatement.
Résultats
Entre 2012 et 2016, 20 patients (14 adultes et 6 enfants) qui présentaient un SHUa et ont été traités par éculizumab. 4 patients étaient dépendants des échanges plasmatiques avant la disponibilité de l’éculizumab et 7 autres ont été traités par échanges plasmatiques avant d’avoir reçu de l’éculizumab, 9 ont été traités d’emblée par éculizumab. 5 patients étaient transplantés rénaux. Le traitement par éculizumab a été diminué chez tous les patients et stoppé chez 17 patients. Tous les enfants ont été mis en rémission après éculizumab et un seul patient adulte était résistant au traitement. Parmi les 19 patients répondeurs, le délai de réponse était de 5 jours pour les plaquettes et de 39 pour la créatinine. Parmi les 13 patients adultes répondeurs 1 était rénal de longue date et la diminution de l’éculizumab s’est traduit par l’apparition de signes histologiques de MAT sur le greffon rénal. 3 des 12 patients qui ont eu un arrêt de l’éculizumab ont expérimenté une rechute à 2 semaines, 3 mois et 12 mois. Le suivi de la cohorte adulte est de 27,4 mois. Parmi les 6 patients pédiatriques, 4 ont eu un arrêt de traitement dont 1 a rechuté. Pour ce patient, une nouvelle rémission a été obtenue et a permis un arrêt de traitement sans rechute ensuite. Pour les 2 autres patients pédiatriques, l’arrêt n’a pas été possible. Le suivi de la cohorte pédiatrique est de 31,4 mois.
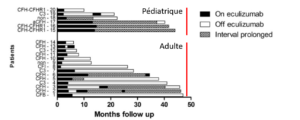
Au total, 5 patients ont rechuté. Grace au suivi rapproché et à la reprise rapide du traitement, aucune séquelle chronique n’a été décrite. 2 de ces 5 patients ont pu avoir un nouvel arrêt du traitement. Les rechutes ont été observées pour 4 patients (sur 8) porteurs d’une mutation du facteur H et 1 patient (sur 4) porteur d’une mutation de C3.
Cette stratégie a permis d‘économiser 11,4 millions d’euros.
Conclusion
Cette étude va à l’encontre des recommandations actuelles d’utilisation de l’éculizumab à vie. Cette stratégie repose cependant sur le rationnel suivant : 1/ il n’existe aucune preuve que ce traitement doive être administré à vie pour éviter une rechute d’autant plus que le traitement utilisé avant, les échanges plasmatiques, pouvait être interrompu sans récidive dans un nombre important de cas de SHUa, 2/ Les conséquences d’utilisation de l’éculizumab à long terme ne sont pas connues, en particuliers les conséquences infectieuses et plus particulièrement le risque de méningites méningococciques, 3/ le risque de récidive dépend de facteurs cliniques, génétiques, de la présence de trigger ou de la dose d’anticalcineurines récue après rejet de greffe. Dans cette cohorte, environ 30% de rechutes ont été observées, sans conséquence chronique, et a permis une réduction du coût du traitement.
Les plus du papier
Cette étude vient questionner les recommandations actuelles sur la durée d’utilisation de l’éculizumab. L’arrêt du traitement, pour peu que le suivi soit strict et que le redémarrage du traitement soi rapide, n’occasionne pas de conséquence. Il est aussi démontré une réduction des coûts dans la prise en charge des SHUa.
Les critiques
Il s’agit d’une petite cohorte. (20 patients), hétérogène tant dans la présentation clinique (adultes et enfants, patients greffés ou non, traitement préalable par échanges plasmatiques ou d’emblée par éculizumab) que par la variété des causes.
Cette étude ouvre la voie à des essais contrôlés ultérieurs pour mieux codifier l’utilisation de l’éculizumab qui a révolutionné le pronostic des SHUa.