BJN#76 Néphropathie et VIH : les nouveautés
Kidney Disease in HIV: Moving beyond HIV-Associated Nephropathy
Revue de la littérature
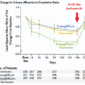
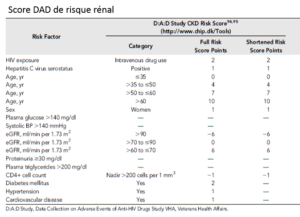
Infection chronique par le VIH : Population restant à haut risque d’IRC. Risque évaluable par Score D.A.D (Figure 1)
Les antirétroviraux restent le traitement de choix des néphropathies induites par le VIH. Les néphropathies induites par le VIH régressent après contrôle de la charge virale (surtout pour l’HIVAN).
Avec la transformation de l’infection par le VIH en maladie chronique et le vieillissement des patients, les causes sous-jacentes majoritaires d’IRC sont passées des causes liées au VIH à celles liées au FDRCV classiques et à la néphrotoxicité des traitements.
La Mutation du gène APOL1
- La mutation du gène APOL1 est associée à un risque majeur de développer une HIVAN en particulier lors de la présence d’un double variant G1/G2 (risque multiplié par un facteur 29 à 89), et chez les sujets Afro-américains
- Risque accru de développer une protéinurie et une MRC chez les sujets VIH mutés
- On retrouve l’expression d’APOL1 dans les podocytes et les cellules endothéliales uniquement. APOL1 permettrait la persistance du VIH dans les podocytes et induirait leur apoptose.
Néphrotoxicité des ARV
3 ARV principalement associés au risque d’IRC :
– TDF : 21 %
– Atazanavir : 16%
– Lopinavir boosté au ritonavir : 8%
Certains ARV : augmentation de la créatinine à l’initiation par diminution de la sécrétion tubulaire de Créatinine (Dolutegravir, Ritonavir, Cobicistat, Rilpivirine)
Tenofovir disoproxil fumarate (TDF) : Elimination rénale : filtration glomérulaire et sécrétion tubulaire
– Associé à une Augmentation du risque d’IRC, protéinurie, diabète insipide néphrogénique
– Mécanisme : Lésions mitochondriales par inhibition de la DNA polymerase gamma
– Atteinte essentiellement tubulaire proximale (Fanconi)
– Risque accru en cas d’association avec IP boostés au Ritonavir (augmentation de l’absorption intestinale et diminution de la sécrétion urinaire du TDF)
– Récupération à l’arrêt du TDF : complète pour la dysfonction tubulaire, parfois incomplète pour la fonction rénale
– Stratégies de prophylaxie pré exposition par le TDF : Associée à une légère dégradation du DFG
Pas d’augmentation du risque de Fanconi (mais adhésion au thérapeutique faible)
Tenofovir alafenamide (TAF) : nouvelle molécule (prodrogue du tenofovir)
– Moins de toxicité rénale que le TDF
– Risque existant mais moindre de protéinurie, mais pas d’aggravation du DFG (mais suivi court (48s) et sujets très sélectionnés)
Atazanavir :
– Associé à une cristallurie, des urolithiases radio-opaques d’atazanavir, des néphrites interstitielles aigues granulomateuses et une insuffisance rénale chronique.
– Facteurs de risque de néphropathie à l’Atazanavir : pH alcalin, IRC, surdosage
– Réversibilité après arrêt non étudiée
Transplantation rénale
Augmentation du nombre de patients VIH transplantés depuis 15 ans (sujets rigoureusement sélectionnés)
- Survie greffon légèrement moins bonne que la population générale greffée
- Mais risque accru de rejet aigu
- Risque d’immunodépression profonde lors de l’utilisation d’ATG en induction
- Facteur de risque majeur de mortalité : Co-infection VHC
- Mais amélioration de la mortalité par rapport aux sujets IRC VIH sur liste d’attente
- Stratégie antirétrovirale chez transplanté rénal optimale incertaine : IP et INNTR inhibiteurs du cytochrome P450 (risque de surdosage en anticalcineurines et inhibiteurs de mTOR)
Quelques résultats satisfaisants de transplantation de donneurs VIH+ sélectionnés chez receveurs VIH+ (Afrique subsaharienne)
Merci à Mickaël Bobot, Interne de Néphrologie à Marseille et membre du Conseil Scientifique du CJN, pour cette synthèse bibliographique. Vous aussi, n’hésitez pas à nous envoyer vos lectures !